 人教版九年級上冊化學初中同步練習及答案(第4單元課題4_式與化合價).doc
人教版九年級上冊化學初中同步練習及答案(第4單元課題4_式與化合價).doc
課題4 化學式與化合價5 分鐘訓練1.標出下列化合物中帶點元素的化合價。KMnO4 K2MnO4 Fe(NO3)2 Na2FeO4NH4NO3Ca(ClO)2HClO4思路解析:本題考查基本化合價。答案:+7+6+2+6-3和+5+1+12.___________________稱為該物質的化學式。思路解析:本題考查化學式的定義。化學式是利用元素符號表示物質組成的式子。答案:利用元素符號表示物質組成的式子3.元素的_______________是體現化合物中不同元素原子數目比值關系的數值。思路解析:本題考查化合價的概念和作用。答案:化合價4._____________稱為離子。化學上常用“____________”來命名。常見的原子團有(OH-)、碳酸根( )、______________( )、____________( )、____________( )等。答案:帶電的原子或原子團根氫氧根CO2-3硫酸根(SO2-4)硝酸根(NO-3)碳酸氫根(HCO-3)(其他合理答案也正確)10分鐘訓練1.在1個H2SO4分子和1個H3PO4分子中,不正確的是( )A.氧的質量分數一樣 B.氧原子個數一樣多C.其相對分子質量一樣 D.硫元素和磷元素的個數一樣多思路解析:硫酸和磷酸的相對分子質量相同,氧的原子個數即氧的質量相同,故氧的質量百分比相同。不能說硫元素和磷元素個數相同,因為元素是宏觀概念。答案:D2.在100個C2H2和100個H2O2分子中,含量相同的是( )A.氫元素 B.含氫的質量分數C.氫原子 D.氫分子思路解析:在H2O2、C2H2中,每個分子都含有兩個氫原子,所以氫原子個數相同。答案:C3.下面敘述不正確的是( )A.元素的化合價是元素的原子在形成化合物時才表現出來的性質B.在氫氣中氫元素的化合價為1C.在水中氧元素的化合價為-2D.在NH3中氮元素的化合價為-3思路解析:在氫氣中,氫元素的化合價為0而不是+1。答案:B4.X、Y兩元素相對原子質量之比34,在X,Y形成化合物的化學式中質量比為38,則該化合物的化學式為( )A.XY B.XY2 C.X2Y D.X2Y3思路解析:設X的相對原子質量為3a,Y的相對原子質量為4a,則X、Y形成化合物的化學式中X、Y的原子個數之比為(3a/3)(8/4a)=12。答案:B30 分鐘訓練1.碳酸氫銨(NH4HCO3)是一種常用的氮肥,其中氮元素的化合價為 ( )A.+5 B.+1 C.-1 D.-3思路解析:根據“化合物中各元素的化合價代數和為零”的原則,可求出NH4HCO3中N元素的化合價為-3。答案:D2.下列計算正確的是( )A.2CO2的相對分子質量總和=212+162=56B.Ca(OH)2的相對分子質量=40+16+12=58 C.(NH4)2SO4的相對分子質量=(14+14)2+32+164=132D.2H2O的相對分子質量總和=212+16=20思路解析:A錯誤,因為在2CO2中共有4個氧原子;B錯誤,在Ca(OH)2中有兩個氧原子,而不是一個氧原子;C正確;D在2H2O中,共有兩個氧原子。答案:C3.下列物質中,硫元素的化合價為+6的是( )A.H2SO4 B.SO2 C.S D.H2SO3思路解析:A中S元素為+6價;B中S元素為+4價;C中S元素為0價;D中S元素為+4價。答案:A4.下列含氮元素的化合物,氮元素化合價最高的是( )A.NO B.NO2 C.N2O5 D.N2O思路解析:A中氮元素化合價為+2,B中氮元素的化合價為+4,C中氮元素化合價為+5;D中氮元素的化合價為+1。答案:C5.下列物質的化學式書寫正確的是( )A.五氧化二磷2PO5 B.氯化鉀KClC.氧化鋁AlO D.高錳酸鉀K2MnO4思路解析:A中五氧化二磷應該寫成P2O5;B正確;C氧化鋁的化學式為Al2O3;D中高錳酸鉀的化學式為KMnO4而不是K2MnO4。答案:B6.在CuSO4中銅元素、硫元素、氧元素的質量比為( )A.212 B.114 C.421 D.121思路解析:CuSO4中銅元素、硫元素、氧元素質量比為643264=212。答案:A7.在二氧化硫中,硫元素的質量分數是( )A.66.7% B.50% C.33.3% D.3.1%思路解析:在二氧化硫中,相對分子質量為64,硫元素的相對原子質量為32,所以硫元素的質量分數為32/64100%=50%。答案:B8.某物質的化學式是R(OH)2,相對分子質量為58,則R的相對原子質量為( )A.24 B.24g C.40 g D.40思路解析:R的相對原子質量為58-2(16+1)=24,無單位。答案:A9.某正三價金屬元素A,它的氧化物中含氧元素的質量分數是30%,則A的相對原子質量是 ( )A.56 B.27 C.32 D.16思路解析:該元素的化合價為+3,則該元素的氧化物的化學式為A2O3,設它的相對原子質量為x,則(316)/(316+2x)=30%,解得:x=56。答案:A10.1985年科學家發現一種新物質,化學式為C60,下列說法中正確的是( )A.該物質是混合物 B.該物質為新型化合物 C.該物質的相對分子質量為120 D.該物質的一個分子中含有60個碳原子思路解析:該物質為含60個碳原子的大分子,相對分子質量為720,是碳的一種單質。答案:D11.下列化合物中,含有相同原子團的是( )A.SO3和H2SO4 B.Cu(OH)2和NaOHC.KMnO4和K2MnO4 D.KClO3和KCl思路解析:B中都含有OH-,其余都不相同。答案:B12.某物質含有A、B兩種元素,已知A、B兩種元素原子的相對原子質量之比為72,經測定該物質A、B兩元素的質量比為73,則該物質的化學式為( )A.A2B3 B.AB2 C.A2B D.A3B2思路解析:令A的相對原子質量為7x,B的相對原子質量為2x,則A、B兩種元素的原子個數比為(7/7x)(3/2x)=23。答案:A13.(1)一個氫原子與一個水分子的質量比是多少?一個水分子與一個二氧化碳分子的質量比是多少?(2)一個水中分子中氫、氧原子質量比是多少?其中氫原子的質量分數是多少?(3)二氧化碳中碳元素的質量分數是多少?思路解析:(1)一個水分子是由2個氫原子與1個氧原子構成的,所以一個水分子的質量是2個氫原子與1個氧原子的質量之和。一個氫原子與一個水分子的質量比為:一個水分子與一個二氧化碳分子的質量比為結論:原子(分子)間質量比,與相對原子(分子)質量比相等。(2)解:m(H)m(O)=2Ar(H)Ar(O)=211618w(H)=100%=100%=11.1%(3)w(C)= 100%=100%=27.3%答案:(1) (2)1811.1%(3)27.3%14.寫出氫、硫、碳、鈉、鎂、鋁、鐵等十種元素的常見化合價并分別寫出它們氧化物的化學式。(1)在上述元素中,哪些元素能結合組成化合物?寫出其中幾種化合物的化學式。(2)依據下列物質名稱寫出化學式:硫酸鈉、碳酸銅、硝酸鎂、三氯化鋁。(3)依據下列物質的化學式寫出名稱:K2SO4、KNO3、Na2CO3、Al(OH)3、(NH4)2SO4。(4)比較三種氮肥的含氮量大小:硫銨、硝銨、尿素CO(NH2)2。(5)要在每畝地上增加1 kg氮元素,問10畝地應施加尿素多少千克。如果改用碳酸氫銨,需要增加多少千克?思路解析:本題考查基本化合物的化學式和基本物質的含量和原子個數比。答案:(1)金屬和非金屬間能夠形成化合物。H2S、CH4、MgS、FeS等。(2)Na2SO4、CuCO3、Mg(NO3)2、AlCl3。(3)硫酸鉀、硝酸鉀、碳酸鈉、氫氧化鋁、硫酸銨。(4)硫酸銨中,氮的含量為28/(28+81+164+32)100%=21.2%。硝銨中氮的含量為35;尿素中氮的含量為47%。故含氮量順序為:尿素硝銨硫銨。(5)增加的尿素的質量為1 kg47%=21.4 kg。如改用NH4HCO3,則需要增加21.4 kg=30.2 kg4
- 關 鍵 詞:
- 人教版 九年級 上冊 化學 初中 同步 練習 答案 單元 課題 化合價
 叮當云教育所有資源均是用戶自行上傳分享,僅供網友學習交流,未經上傳用戶書面授權,請勿作他用。
叮當云教育所有資源均是用戶自行上傳分享,僅供網友學習交流,未經上傳用戶書面授權,請勿作他用。 關于本文
相關資源
 人教版九年級上冊化學第6單元 課題2碳的氧化物.pptx
人教版九年級上冊化學第6單元 課題2碳的氧化物.pptx  人教版九年級上冊化學第6單元 課題2 碳的氧化物學習任務單.docx
人教版九年級上冊化學第6單元 課題2 碳的氧化物學習任務單.docx  人教版九年級上冊化學第6單元 課題2 碳的氧化物教學設計.docx
人教版九年級上冊化學第6單元 課題2 碳的氧化物教學設計.docx  人教版九年級上冊化學第6單元 課題2 碳的氧化物作業練習.docx
人教版九年級上冊化學第6單元 課題2 碳的氧化物作業練習.docx  人教版九年級上化學第6單元課題2《碳的化合物》課件+教學設計+學習單+課后練習.rar
人教版九年級上化學第6單元課題2《碳的化合物》課件+教學設計+學習單+課后練習.rar  2019-2020學年廣東省廣州市從化區九年級(上)期末化學試卷(含答案).docx
2019-2020學年廣東省廣州市從化區九年級(上)期末化學試卷(含答案).docx  2019-2020學年廣東省廣州市白云區九年級(上)期末化學試卷(含答案).docx
2019-2020學年廣東省廣州市白云區九年級(上)期末化學試卷(含答案).docx  2019-2020學年廣東省廣州市番禺區九年級(上)期末化學試卷(含答案).docx
2019-2020學年廣東省廣州市番禺區九年級(上)期末化學試卷(含答案).docx  2019-2020學年廣東省廣州市海珠區九年級(上)期末化學試卷(含答案).docx
2019-2020學年廣東省廣州市海珠區九年級(上)期末化學試卷(含答案).docx  2019-2020學年廣東省廣州市花都區九年級(上)期末化學試卷(含答案).docx
2019-2020學年廣東省廣州市花都區九年級(上)期末化學試卷(含答案).docx 


 24秋新一年級上冊語文2 江南(朗讀音頻).mp3
24秋新一年級上冊語文2 江南(朗讀音頻).mp3  贛科版六年級下冊信息科技第10課 主題活動:空調中的控制 教案.doc
贛科版六年級下冊信息科技第10課 主題活動:空調中的控制 教案.doc 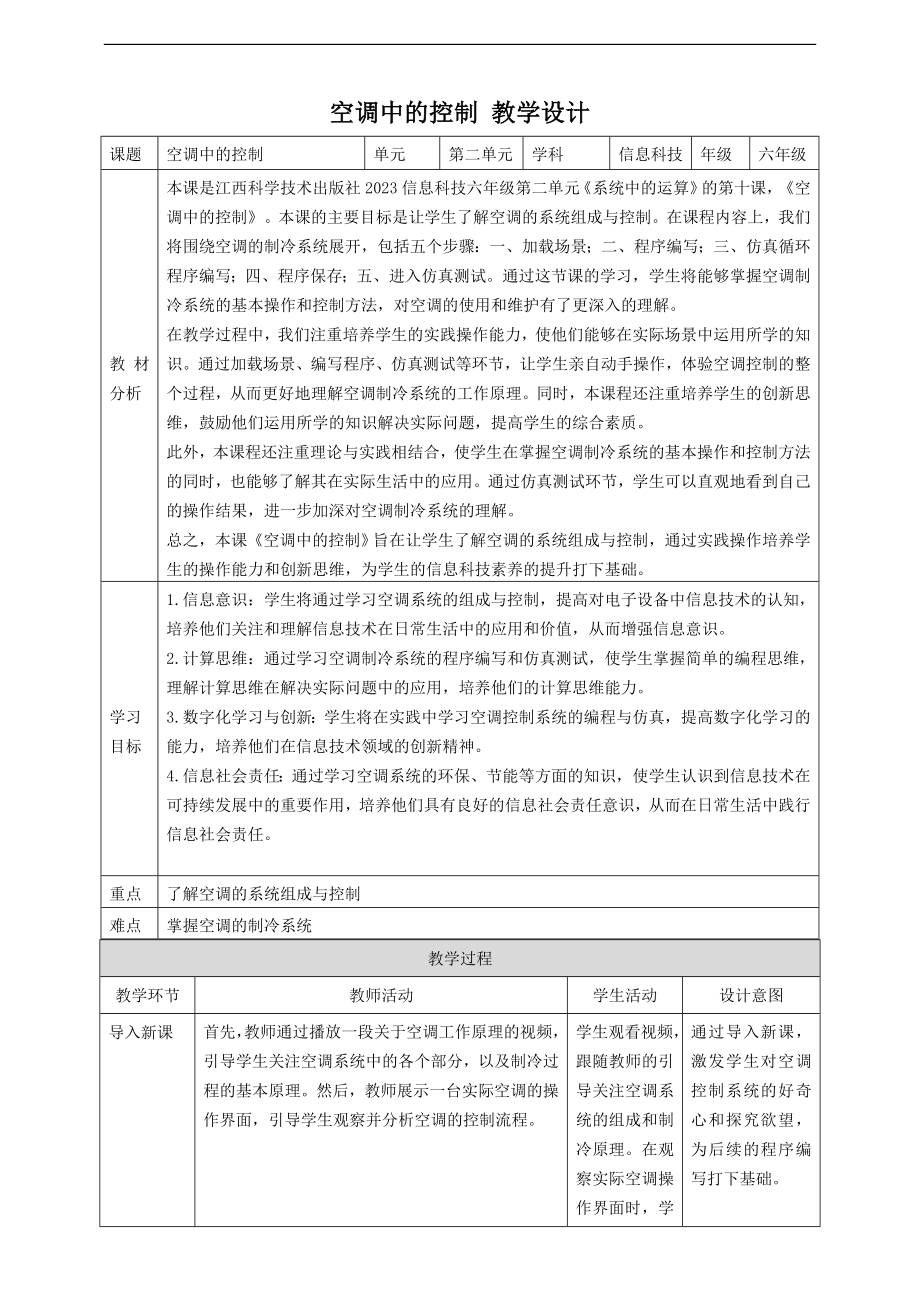 贛科版六年級下冊信息科技教案(全冊教學設計打包下載).rar
贛科版六年級下冊信息科技教案(全冊教學設計打包下載).rar 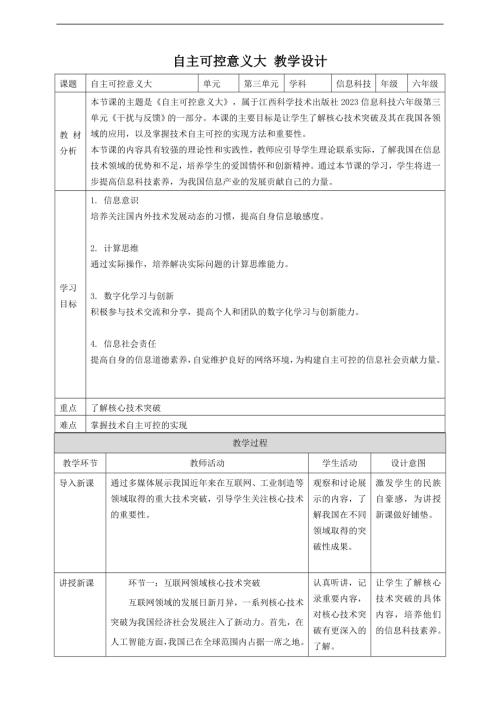 贛科版六年級下冊信息科技第14課 自主可控意義大 教案.doc
贛科版六年級下冊信息科技第14課 自主可控意義大 教案.doc  贛科版六年級下冊信息科技15 跨學科主題:小型擴音系統 課件(共16張PPT) .pptx
贛科版六年級下冊信息科技15 跨學科主題:小型擴音系統 課件(共16張PPT) .pptx 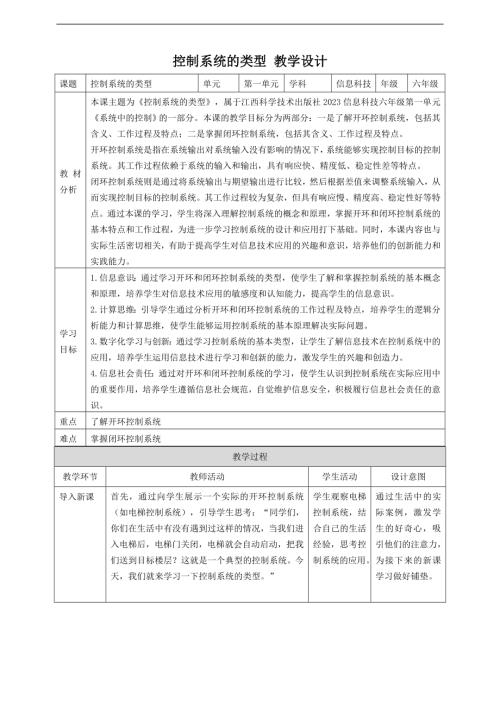 贛科版六年級下冊信息科技第4課 控制系統的類型 教案.doc
贛科版六年級下冊信息科技第4課 控制系統的類型 教案.doc  贛科版六年級下冊信息科技第11課 控制系統中的干擾 教案.doc
贛科版六年級下冊信息科技第11課 控制系統中的干擾 教案.doc  贛科版六年級下冊信息科技11控制系統中的干擾 課件(共22張PPT).pptx
贛科版六年級下冊信息科技11控制系統中的干擾 課件(共22張PPT).pptx 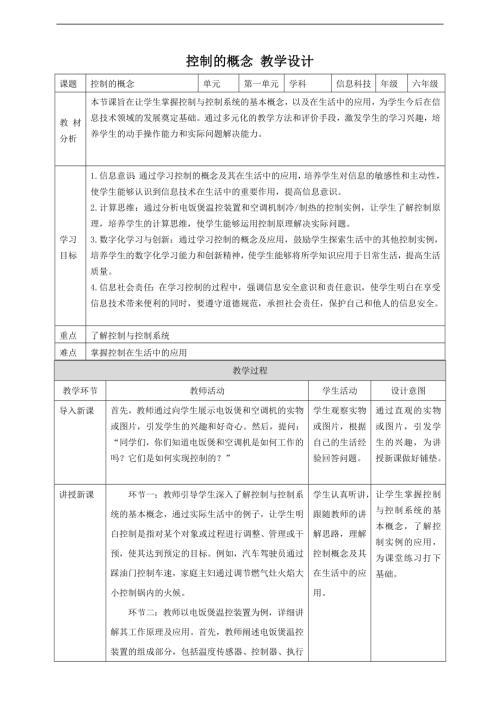 贛科版六年級下冊信息科技第1課 控制的概念 教案.doc
贛科版六年級下冊信息科技第1課 控制的概念 教案.doc  贛科版六年級下冊信息科技14 自主可控意義大 課件(共23張PPT) .pptx
贛科版六年級下冊信息科技14 自主可控意義大 課件(共23張PPT) .pptx  贛科版六年級下冊信息科技第5課 主題活動:汽車定速巡航 教案.doc
贛科版六年級下冊信息科技第5課 主題活動:汽車定速巡航 教案.doc  贛科版六年級下冊信息科技第12課 反饋概述 教案.doc
贛科版六年級下冊信息科技第12課 反饋概述 教案.doc  贛科版六年級下冊信息科技10 主題活動:空調中的控制 課件(共16張PPT) .pptx
贛科版六年級下冊信息科技10 主題活動:空調中的控制 課件(共16張PPT) .pptx  贛科版六年級下冊信息科技第2課 控制的分類 教案.doc
贛科版六年級下冊信息科技第2課 控制的分類 教案.doc  贛科版六年級下冊信息科技13 反饋的類型 課件(共17張PPT) .pptx
贛科版六年級下冊信息科技13 反饋的類型 課件(共17張PPT) .pptx  贛科版六年級下冊信息科技第5課 主題活動:汽車定速巡航 課件(共15張PPT) .pptx
贛科版六年級下冊信息科技第5課 主題活動:汽車定速巡航 課件(共15張PPT) .pptx 
